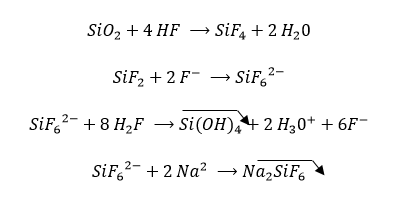Una arenisca esta compuesta de granos de diferentes tamaños y también de diferentes composiciones. Los granos gruesos forman la matriz y son principalmente de cuarzo y feldespatos.
En los espacios entre granos gruesos, o sea en los poros, se encuentran partículas de diámetro muy chico, los finos, que pueden ser arcillas, carbonatos o granos muy finos de cuarzo.
Estos finos tapan parcialmente los poros e impiden el movimiento del fluido dentro de la matriz. En un tratamiento matricial, se busca remover los finos que están en los poros.
Pero se debe olvidar que estos mismos finos tienen como efecto el pegado de los granos entre sí, consolidando la formación.
Si se disuelven por completo, se puede desconsolidar a la formación. Esto sería otro motivo de daño irreversible.
La solubilidad de cada mineral depende de la relación área de contacto versus volumen de material, y depende de su posición dentro de la roca, lo que definirá la posibilidad de contacto con el fluido de tratamiento.
Por eso, en estudios de laboratorio se debe determinar la composición mineralógica de la roca (ensayos de difracción por rayos X), y también determinar la posición de cada elemento (estudio de láminas finas o microscopio electrónico).
En la Tabla 1 se ha resumido la solubilidad en HCl y HF de los componentes más comúnmente encontrados en una arenisca.
También se expone de una comparación relativa de su área de contacto. Los granos de feldespatos y cuarzo, que son los granos que forman la matriz tienen una superficie de contacto muy chica comparada con su volumen, pero las arcillas tienen una superficie de contacto muy grande.
Un gramo de kaolinita tiene una superficie de contacto de 22 m², o sea su posibilidad de reaccionar con el ácido va ser mucho mayor.
| Mineral | Área de Contacto | HCl | HCl-HF |
|---|---|---|---|
| Cuarzos | Muy baja | No | Muy baja |
| Chert | Baja a Moderada | No | Baja a moderada |
| K. Feldespatos | Baja a Moderada | Muy baja | Baja a moderada |
| Micas | Baja | Muy Baja | Baja a moderada |
| Kaolinita | Alta | Baja | Alta |
| Ilita | Muy alta | Baja | Alta |
| Esmectita | Alta | Baja | Alta |
| Clorita | Alta | Moderada | Alta |
| Zeolita | Alta | Alta a moderada | Alta |
| Calcita | Baja a moderada | Muy alta | Muy alta + CaF2 |
| Dolomita | Baja a moderada | Muy alta | Muy alta + CaF2 |
Prácticamente todas las rocas tienen algo de solubilidad en HCl. Algunas pueden ser consideradas insolubles a baja temperatura, pero a alta temperatura todas terminan siendo parcialmente solubles.
Algunos de los materiales, como la calcita y la dolomita que son solubles en clorhídrico y en fluorhídrico tienen el inconveniente que, por efectos de reacciones secundarias después del contacto con HF, puede re-precipitar formando otro material insoluble.
Si la reacción del HCl con las arcillas es lenta a temperatura normal, la reacción del fluorhídrico es muy rápida.
Esta alta velocidad de reacción puede ser una desventaja ya que todo el ácido reacciona en la vecindad del pozo, donde desconsolida la formación y no llega lo suficientemente lejos dentro de la matriz.
Las reacciones más comunes al ácido clorhídrico se pueden observar a continuación:
El HCl reacciona con los carbonatos pero luego se generan precipitados. Entonces es necesario disolver todos los carbonatos antes de que el HF entre en la formación. Es la razón por la cual siempre se deberá utilizar primero un colchón con el HCl antes de bombear el HF.
El HCl es también utilizado como post flujo para separar el HF de sales que puedan estar en los fluidos de terminación o de inyección, ya que el HF reacciona con iones como el potasio (K⁺) y forman otro tipo de precipitado.
El ácido clorhídrico comercial viene con concentraciones de 28 a 35%, pero para los tratamientos en areniscas se utilizan comúnmente de 10 a 15% en el preflujo y de 5% en el post flujo.
Como referencia podemos decir:
- 1.000 galones de HCl al 15% disuelven 1.840 lb de CaCO₃.
- 1.000 litros de HCl al 15% disuelven 220 Kg de CaCO₃.
- El pH (-log[H⁺]) del HCl al 15% es -0.64.
El cuarzo se presenta en formación como clastos (granos) pero también como finos. Su reactividad con el ácido fluorhídrico dependerá del tamaño de las partículas y de la relación superficie de contacto versus volumen.
El HF disuelve el cuarzo (SiO₂), pero disuelve también los demás compuestos alumino-silicato y por supuesto disuelve también todo lo que es soluble en HCl.
Las reacciones del HF son muy complejas y se complican más aún con la composición de los distintos componentes de la arenisca.
Parte de los subproductos de la reacción están diluidos en el ácido gastado pueden luego formar precipitados, algunos de los cuales son materiales insolubles.
El calcio y el magnesio forman fluoruros (CaF₂, MgF₂), el potasio y el sodio forman sales de fluorsilicatos (Na₂SiF₆, K₂SiF₆).
Estos productos son insolubles y taponan completamente la matriz. El Si(OH)₄ (gel de sílice) es un material amorfo que se deposita en forma de película sobre la matriz y sobre las arcillas. Tiene como efecto retardar la reacción.
Hasta hace poco se pensaba que su precipitación generaba un daño importante pero hoy se sabe que forma una película sobre los clastos y que prácticamente no tapa la matriz.
Estadísticas hechas con datos de campo muestran volúmenes de 125 a 200 gal/pie (1.500 a 2.500 lt/m) de HF dan una relación de éxitos aceptables.
Esta es una regla de dedo que puede ser utilizada cuando no hay más información pero se recomienda hacer un estudio caso por caso.
Como referencia podemos decir:
- 1.000 galones de HCl-HF al 12-3% disuelven 500 lb de limo y arcilla (o sea 1.000 lt disuelve 60 Kg.).
- El HF es normalmente preparado disolviendo bifloruoruro de amonio en HCl.
- (123 lb de NH₄HF₂ + 1.000 gal de 1% HCL = 1.000 gal de 1% HF).
La ecuación de la reacción del HF con el cuarzo es sencilla, pero las reacciones con los aluminosilicatos son mucho más complejas. Se produce una primera reacción.
Después con el tiempo y la temperatura los subproductos de esta reacción son reactivos de una segunda y una tercera reacción, y cada reacción deja subproductos en solución, algunos de los cuales precipitan. Las reacciones del HF con aluminio-silicatos las podemos observar a continuación:
Primaria:
Donde:
- x = 1 a 3
- M = (K, Na, Mg, Ca, Fe, …)
Secundaria (T> 75⁰F – 24⁰C):

Terciaria (f{T, relación HCl/HF}, pH<3):

Donde:
- y < x
H₃AIF₆ se gasta en el precipitado de AIF₃ y Al(OH)₃
Estas reacciones generales son solamente indicativas ya que no están balanceadas. Uno de los subproductos de las reacciones es un ión de silicon inestable (HSiF₅).
Con temperatura este se hidroliza a ácido fluosilícico (H₂SiF₆), un ácido fuerte que actúa en las reacciones secundarias.
La distribución de material da una relación F/Si de alrededor de 5, siendo HSiF₅ el material principal. Los aluminos se disuelven en mezclas de fluoruro de aluminio (AIF²⁺, AlF₂⁺, AIF₃).
La relación F/Al, x, es dependiente de la concentración de HCl presente en el momento de cada una de las reacciones, y es también dependiente de la composición mineralógica de la formación.
A mayor concentración de HCl menor relación F/Al, y mayor eficiencia para disolver los alumino-silicatos. Las reacciones secundarias aparecen a una temperatura superior a los 75⁰F (24⁰C), o sea en condiciones de yacimiento: siempre.
Las reacciones terciarias son dependientes de la relación HCl/HF, de la temperatura y acontecen a pH inferior a 3.
Según el tipo de daño, el fluido de formación, la temperatura, se deberá elegir entre varias mezclas de ácidos. La elección dependerá del objetivo de cada tratamiento.
El sistema más utilizado está basado en mezclas de HCl y HF, y normalmente se compone de varias etapas. Para definir el tratamiento se puede seguir un árbol de decisión como el que se presenta en la Figura 1.
La primera condición que se verifica es la permeabilidad de la formación: si la capa es de muy baja permeabilidad se prefiere un tratamiento de fractura y no un tratamiento matricial.
Como segunda opción se debe considerar el porcentaje de carbonato presente en la roca. Si hay mucho carbonato en la arenisca esto significa que se debería bombear un volumen importante de HCl adelante del HF para asegurar la disolución de todos los carbonatos.
Esta disolución ya sería una estimulación por sí misma, y no garantizaría haber disuelto todo. En el caso de definir el uso de HF entonces se debe conocer la cantidad de finos presentes, si estos finos pueden migrar o no, etc.
Se puede usar este árbol de decisión o árboles más completos como los que se encuentran en los simuladores.

Si te ha gustado este artículo y sientes que aporta valor, te invitamos a compartirlo en tus redes sociales preferidas, así nos ayudas a difundir información a todo a quien pueda interesar. Si tienes alguna duda, comentario o sugerencia, puedes dejarlo abajo en la sección de comentarios. ¡Nos interesa tu opinión!